ປະຕິກິລິຍາຂອງທາດປະສົມ mercury
mercury ໂລຫະແລະທາດປະສົມຂອງມັນແມ່ນເປັນພິດສູງຕໍ່ສິ່ງມີຊີວິດ. ນີ້ແມ່ນຄວາມຈິງໂດຍສະເພາະສໍາລັບທາດປະສົມທີ່ລະລາຍສູງໃນນ້ໍາ. ຕ້ອງເອົາໃຈໃສ່ຢ່າງລະມັດລະວັງໃນເວລາທີ່ທົດລອງປະສົມປະສານຂອງອົງປະກອບທີ່ເປັນເອກະລັກນີ້ (mercury ແມ່ນໂລຫະດຽວທີ່ເປັນຂອງແຫຼວຢູ່ໃນອຸນຫະພູມຫ້ອງ). ການປະຕິບັດຕາມຫຼັກການພື້ນຖານຂອງນັກເຄມີບໍ? ຈະຊ່ວຍໃຫ້ທ່ານສາມາດດໍາເນີນການທົດລອງຫຼາຍໆຢ່າງດ້ວຍສານປະກອບ mercury ໄດ້ຢ່າງປອດໄພ.
ໃນການທົດລອງຄັ້ງທໍາອິດ, ພວກເຮົາໄດ້ຮັບການ amalgam ອາລູມິນຽມ (ການແກ້ໄຂຂອງໂລຫະນີ້ໃນທາດປຣອດຂອງແຫຼວ). Mercury (II) solution Hg nitrate (V) Hg (NO3)2 ແລະສິ້ນຂອງສາຍອາລູມິນຽມ (ຮູບ 1). ແທ່ງອາລູມິນຽມ (ຖືກອະນາໄມຢ່າງລະມັດລະວັງຂອງເງິນຝາກ) ຖືກໃສ່ໃນທໍ່ທົດລອງທີ່ມີການແກ້ໄຂຂອງເກືອ mercury ທີ່ລະລາຍ (ຮູບ 2). ຫຼັງຈາກເວລາໃດຫນຶ່ງ, ພວກເຮົາສາມາດສັງເກດເຫັນການປ່ອຍຟອງອາຍແກັສຈາກຫນ້າດິນຂອງສາຍ (ຮູບ 3 ແລະ 4). ຫຼັງຈາກທີ່ເອົາ rod ອອກຈາກການແກ້ໄຂ, ມັນ turns ໃຫ້ເຫັນວ່າດິນເຜົາໄດ້ຖືກປົກຫຸ້ມດ້ວຍ fluffy ເຄືອບ, ແລະນອກຈາກນັ້ນ, ພວກເຮົາຍັງເຫັນບານຂອງ mercury ໂລຫະ (ຮູບ 5 ແລະ 6).
ເຄມີສາດ - ປະສົບການຂອງການສົມທົບ mercury ໄດ້
ພາຍໃຕ້ສະພາບປົກກະຕິ, ພື້ນຜິວຂອງອາລູມິນຽມຖືກເຄືອບດ້ວຍຊັ້ນຂອງອາລູມິນຽມອອກໄຊທີ່ແຫນ້ນຫນາ.2O3ແຍກໂລຫະຢ່າງມີປະສິດທິພາບຈາກອິດທິພົນສິ່ງແວດລ້ອມທີ່ຮຸກຮານ. ຫຼັງຈາກທໍາຄວາມສະອາດແລະ immersing rod ໃນການແກ້ໄຂຂອງເກືອ mercury, Hg ions ຖືກຍ້າຍອອກໄປ.2+ ອາລູມິນຽມທີ່ມີການເຄື່ອນໄຫວຫຼາຍ
ທາດ Mercury ທີ່ຝາກໄວ້ຢູ່ດ້ານຂອງ rod ປະກອບເປັນປະສົມກັບອາລູມິນຽມ, ເຊິ່ງເຮັດໃຫ້ມັນຍາກສໍາລັບ oxide ທີ່ຈະຍຶດຕິດກັບມັນ. ອະລູມິນຽມເປັນໂລຫະທີ່ມີການເຄື່ອນໄຫວຫຼາຍ (ມັນ reacts ກັບນ້ໍາເພື່ອປ່ອຍ hydrogen - ຟອງອາຍແກັສໄດ້ຖືກສັງເກດເຫັນ), ແລະການນໍາໃຊ້ຂອງມັນເປັນວັດສະດຸໂຄງສ້າງແມ່ນເປັນໄປໄດ້ເນື່ອງຈາກການເຄືອບ oxide ຫນາແຫນ້ນ.
ໃນການທົດລອງທີສອງ, ພວກເຮົາຈະກວດພົບ ammonium NH ions.4+ ການນໍາໃຊ້ reagent ຂອງ Nessler (ນັກເຄມີສາດຊາວເຢຍລະມັນ Julius Nessler ເປັນຜູ້ທໍາອິດທີ່ໃຊ້ໃນການວິເຄາະໃນປີ 1856).
ການທົດລອງກ່ຽວກັບປະຕິກິລິຍາຂອງ hops ແລະທາດປະສົມ mercury
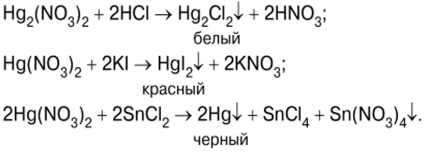
ການທົດສອບເລີ່ມຕົ້ນທີ່ມີການຕົກຂອງພະລັງງານ mercury (II) iodide HgI.2, ຫຼັງຈາກປະສົມການແກ້ໄຂຂອງ potassium iodide KI ແລະ mercury (II) nitrate (V) Hg (NO.3)2 (ຮູບ 7):
ຝົນສີສົ້ມ-ສີແດງຂອງ HgI2 (ຮູບທີ 8) ຫຼັງຈາກນັ້ນ, ປິ່ນປົວດ້ວຍການແກ້ໄຂໂພແທດຊຽມ ໄອໂອດິນ ຫຼາຍເກີນໄປ ເພື່ອໃຫ້ໄດ້ສານປະສົມທີ່ລະລາຍຂອງສູດ K.2HgI4 ? Potassium tetraiodercurate (II) (ຮູບ 9), ເຊິ່ງແມ່ນ reagent ຂອງ Nessler:
ດ້ວຍສານປະສົມທີ່ເປັນຜົນ, ພວກເຮົາສາມາດກວດພົບ ions ammonium. ການແກ້ໄຂຂອງ sodium hydroxide NaOH ແລະ ammonium chloride NH ຈະຍັງຕ້ອງການ.4Cl (ຮູບ 10). ຫຼັງຈາກຕື່ມການແກ້ໄຂເກືອ ammonium ຈໍານວນນ້ອຍໆໃສ່ Nessler reagent ແລະ alkalizing ຂະຫນາດກາງທີ່ມີພື້ນຖານທີ່ເຂັ້ມແຂງ, ພວກເຮົາສັງເກດເຫັນການສ້າງຕັ້ງຂອງສີເຫຼືອງ, ສີສົ້ມຂອງເນື້ອໃນທໍ່ທົດສອບ. ປະຕິກິລິຍາໃນປະຈຸບັນສາມາດຂຽນເປັນ:
ທາດປະສົມ mercury ຜົນໄດ້ຮັບມີໂຄງສ້າງທີ່ສັບສົນ:
ການທົດສອບ Nessler ທີ່ມີຄວາມອ່ອນໄຫວສູງຖືກນໍາໃຊ້ເພື່ອກວດຫາແມ້ກະທັ້ງຮ່ອງຮອຍຂອງເກືອ ammonium ຫຼື ammonia ໃນນ້ໍາ (ເຊັ່ນ: ນ້ໍາປະປາ).

